【前沿速递】病毒病所揭示我国罕见型诺如病毒暴发的分子机制
诺如病毒(Norovirus,NV)是导致全球急性非细菌性胃肠炎暴发的主要病原体之一,在全球范围内多次广泛流行,给人类社会造成了严重的疾病负担。此前,中国疾控中心病毒病所段招军研究员团队报道了一种以前较少发现的诺如病毒GII.P16-GII.2成为我国2016-2017年胃肠炎暴发疫情中的主要致病病原(Ao, et al., Emerg Infect Dis. 2017 Jul; 23:1172-1175. IF=8.222),近期,该研究团队进一步对此次流行GII.P16-GII.2诺如病毒的起源、传播、进化动力学及其流行暴发可能分子机制进行了综合研究,相关研究成果以Genetic Analysis of Re-Emerging GII.P16-GII.2 Noroviruses in 2016-2017 in China为题,在线发表于国际传染病期刊Journal of Infectious Diseases上。


研究背景
诺如病毒(Norovirus,NV)是杯状病毒科的一种单股正链RNA病毒,是导致全球急性非细菌性胃肠炎暴发的主要病原体之一,在全球范围内多次暴发流行。该病毒具有高度的遗传变异性,根据病毒VP1蛋白氨基酸序列同源性不同,诺如病毒可进一步分为GI-GVII七个基因组(Genogroup)和30多个不同的基因型(Genotype)。
在过去二十年间,诺如病毒暴发疫情主要由GII中第4基因型(GII.4)引起。而在2014-2015年,罕见型GII.17取代了GII.4,成为中国及亚洲部分地区诺如病毒疫情暴发的主要病原体。
016至2017年,另一种以前较少发现的诺如病毒GII.P16-GII.2突然代替了先前流行GII.4和GII.17,成为了我国胃肠炎暴发疫情中的主要致病病原。同时,中国香港和台湾、日本、德国、法国、意大利、澳大利亚和美国等地相继报道了该型诺如病毒引起的暴发疫情,提示该病毒已经在世界范围内快速传播流行。但是该病毒的起源、传播、进化动力学及引起暴发流行分子机制目前还不清楚。
结果速览
1. 进化分析发现此次暴发GII.P16-GII.2诺如病毒最有可能起源于2011-2012年流行的GII.P16-GII.2病毒(图1)。相比于先前GII.2诺如病毒,此次流行GII.2病毒进化速率加快(图2)。另外,进化分析显示广东可能为该型诺如病毒暴发流行中心,与先前GII.17流行中心(香港)相近,都位于珠江三角洲区域。
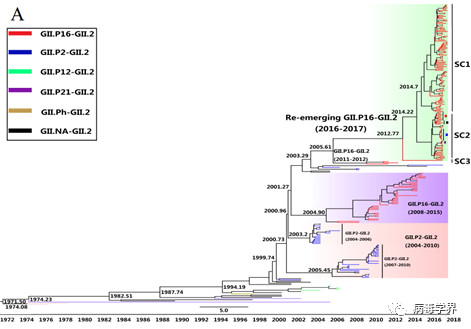
图1. 2016-2017 GII.P16-GII.2诺如病毒VP1基因序列进化树分析
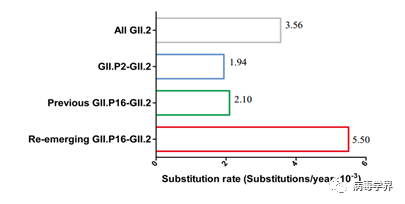
图2. GII.2诺如病毒VP1基因序列进化速率分析
2. 序列分析和唾液结合实验显示此次流行GII.P16-GII.2诺如病毒的抗原性和组织血型抗原(HBGA)受体结合特性类似于先前流行GII.2病毒(图3A和3C)。但是,序列分析发现其非结构蛋白中少量氨基酸发生了突变,特别是聚合酶功能区的氨基酸突变(图4),该突变可能导致了聚合酶功能的变化,进而加快了病毒进化速率。
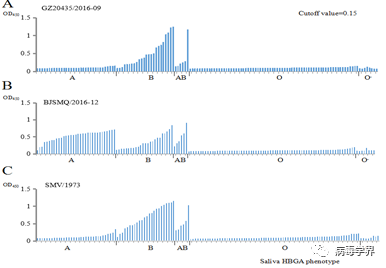
图3. GII.2诺如病毒唾液组织血型抗原结合实验
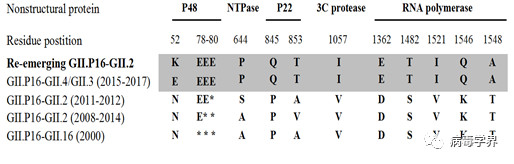
图4. GII.P16-GII.2 诺如病毒非结构蛋白突变序列分析
3. 在暴发的中期,发现了一个GII.P16-GII.2变异株,其HBGA结合谱增加(图3B)。进一步序列分析显示此变异株VP1蛋白相比于早期株发生了一个氨基酸突变Val256Ile,同时晶体结构显示该变异株中在HBGA受体结合区中起重要作用的Asp382发生了方向改变,更倾向于受体结合区域(图5)。Asp382方向改变和Val256Ile突变很可能是导致该变异株HBGA受体结合谱增加的原因。
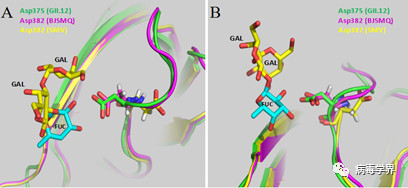
图5. GII.P16-GII.2诺如病毒BJSMQ P dimer 晶体结构分析
结语
本研究结果提示了病毒非结构蛋白氨基酸位点的突变很可能是导致2016-2017年GII.P16-GII.2诺如病毒突然暴发流行的主要原因;且提示了在全球范围内长期开展罕见型诺如病毒监测的重要性,特别是中国珠江三角州区域。
博士生敖元云和丛鑫为论文共同第一作者,段招军研究员为论文通讯作者。中国科学院武汉病毒所崔杰研究员,中国科学院微生物所齐建勋研究员和美国辛辛那提儿童医院医疗中心谭明教授为论文贡献作者。
ABSTRACT
BACKGROUND:
During 2016-2017, the previously rare GII.P16-GII.2 norovirus suddenly emerged as the predominant genotype causing gastroenteritis outbreaksin China and other countries. Its origin, phylodynamics, and mechanism behind the predominance remain unclear.
METHODS:
Bayesian phylogenetic analyses were performed on 180 fullcapsid and 150 polymerase sequences of 2016-2017 GII.P16-GII.2 noroviruses inChina, and those for all publicly available GII.P16 and GII.2 sequences.Saliva-based histo-blood group antigen (HBGA) binding assays and crystalstructural analysis were conducted by the P proteins of 2016-2017 GII.P16-GII.2 noroviruses.
RESULTS:
The re-emerging GII.P16-GII.2 norovirus showed a rapid genetic diversification, after its emergence in 2012-2013. The antigenicity and HBGA binding profile of the early 2016-2017 and pre-2016 GII.2 noroviruses were similar. A further variant with a single Val256Ile mutation and the conventionally orientated Asp382 in VP1 protein showed an expanded HBGA-binding spectrum. Mutations on the surface of polymerase that could alter its function were seen, which may help to accelerate the VP1 gene evolution to 5.5 × 10-3 substitutions/site/year. This virus can be traced back to Pearl River Delta, China.
CONCLUSIONS:
Our findings provide newinsights into GII.2 norovirus epidemics and highlight the necessity of enhanced global surveillance for potential epidemics of rare genotype noroviruses.
参考文献:
1. Ao Y, Cong X, Jin M, Sun X, Wei X, Wang J,Zhang Q, Song J, Yu J, Cui J, Qi J, Tan M, Duan Z. Genetic Analysis of Re-Emerging GII.P16-GII.2 Noroviruses in 2016-2017 in China. J Infect Dis.2018 Mar 29.
doi: 10.1093/infdis/jiy182.
2.Ao Y, Wang J, Ling H, He Y, Dong X, Wang X, PengJ, Zhang H, Jin M, Duan Z. Norovirus GII.P16/GII.2-Associated Gastroenteritis, China, 2016. Emerg Infect Dis. 2017 Jul; 23(7):1172-1175.
doi: 10.3201/eid2307.170034.
3.【EID】中国疾控中心病毒病所段招军研究团队首次报道我国罕见重组诺如病毒。
https://www.sohu.com/a/139682189_749000
内容来源:病毒学界