科学家研发新型寨卡病毒疫苗,有效对抗病毒感染
导读
寨卡病毒(Zika virus,ZIKV)于1947年首次在乌干达恒河猴中发现,属于黄病毒科黄病毒属,为单股正链RNA病毒,主要通过蚊媒传播。近年来,ZIKV在南美、东南亚等地区爆发流行,已造成数百万人感染,尤其是ZIKV感染导致的新生儿小头畸形和格林-巴利综合征,已成为全球公共卫生的新挑战,但目前尚无批准使用的预防疫苗。
近日,美国俄亥俄州立大学大学、德克萨斯州立大学等科学家联合攻关,以减毒重组水疱性口炎病毒(rVSV)为载体,研发了一种表达ZIKV prM-E-NS1多蛋白的病毒载体疫苗,单针免疫便可诱导小鼠产生ZIKV特异性体液和细胞免疫应答,并能有效对抗ZIKV的攻击。相关研究以“A Zika virus vaccine expressingpremembrane-envelope-NS1 polyprotein.”为题,发表于2018年8月3日最新一期的国际期刊Nature Communication。
Science Daily 发布题为“新型疫苗对寨卡病毒具有强大的抵抗”(Novel vaccine approach proves powerful against Zikavirus)的新闻评论,称颂其为“一种独特的针对寨卡疫苗设计”(A uniquely designed experimental vaccineagainst Zika virus has proven powerful in mice, new research has found)。

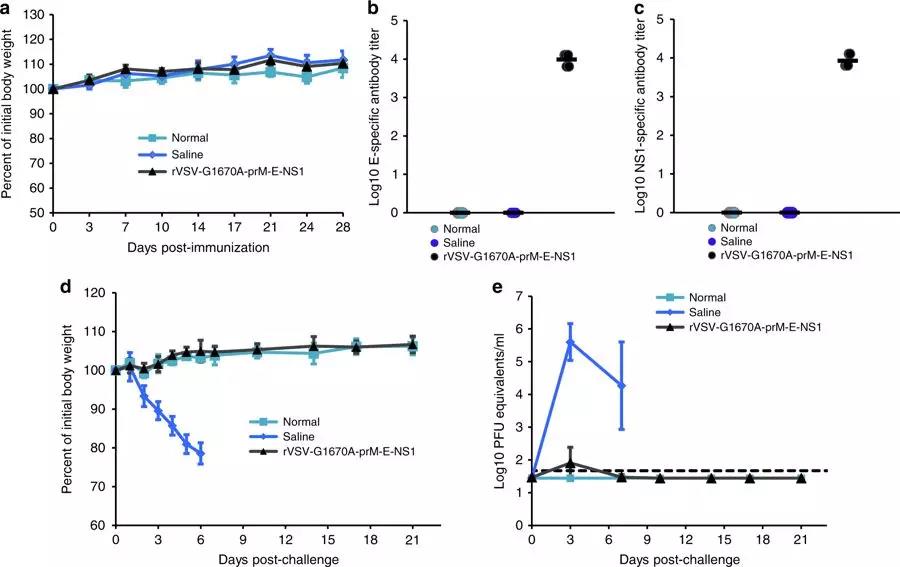
Fig .Validation the safety and immunogenicity of rVSV-prM-E-NS1 in A129 mice
研究背景
寨卡病毒(Zika virus,ZIKV)于1947年首次在乌干达恒河猴中发现,属于黄病毒科黄病毒属,为单股正链RNA病毒,主要通过蚊媒传播。近年来,ZIKV在南美、东南亚等地区爆发流行,已造成数百万人感染,尤其是ZIKV感染导致的新生儿小头畸形和格林-巴利综合征,已成为全球公共卫生的新挑战,但目前尚无批准使用的预防疫苗。
最近报道了几种ZIKV候选疫苗,包括核酸(DNA和mRNA)、灭活病毒、亚基、VLP、病毒载体疫苗(包括腺病毒和痘病毒)和减毒活疫苗。这些候选疫苗在啮齿动物和/或非人类灵长类动物模型中引发了不同程度的体液和细胞免疫和保护。在这些候选疫苗中,DNA疫苗、亚单位疫苗和灭活疫苗已经开始用于临床试验。尽管这些候选疫苗很有希望,但还需要探索其他新的、高效的ZIKV疫苗。
目前寨卡病毒亚基疫苗的研发主要集中在前体膜蛋白(pre-membrane, prM)和包膜蛋白(envelope, E)为抗原靶标,但对非结构蛋白1(non-structual protein 1,NS1)在寨卡病毒特异性免疫应答和保护中的作用知之甚少。
结果速览
1、为了比较不同抗原的免疫原性,作者构建了表达ZIKV不同抗原的13个重组rVZV病毒。设计的抗原结构包括全长E蛋白,删除跨膜区的E蛋白,prM-E结构、信号肽的增减、以及包括同时表达prM-E-NS1多蛋白的抗原的结构,并对这些重组病毒的蚀斑形成大小、生长特性、目的蛋白表达水平、表达产物的电镜分析、小鼠中诱发的抗体水平等特点进行了鉴定。结果显示,prM-E-NS1的rVZV病毒载体中的prM、E、NS1蛋白均能在细胞中进行有效表达,电镜下观察到表达产物形成的VLP颗粒,重组疫苗在小鼠中毒力减弱、具有良好的安全性,单针免疫后1-2周就可引发高水平的血清抗体反应(Fig1)
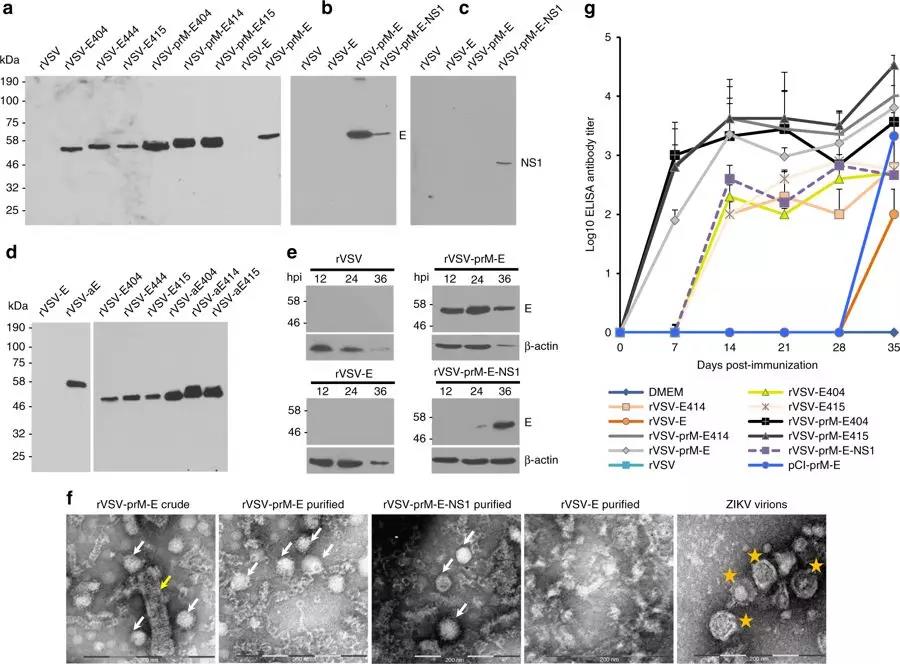
Fig. 1 Recombinant rVSV expressing ZIKV antigens are immunogenic in mice.
2.为了进一步提高疫苗的安全性,研究者对rVZV进行了定点突变的减毒改造,并对获得减毒后的重组载体病毒疫苗rVSV-G1670A-E, rVSV-G1670A-E, rVSV-G1670A-prM-E和rVSV-G1670A-prM-E-NS1与野生型病毒rVZV和母本病毒rVSV-G1670A进行了比较。结果表明,基于突变载体MTase-defective rVSV (mtdVSV)的疫苗具有高度的减毒性和良好的免疫原性(Fig2)。
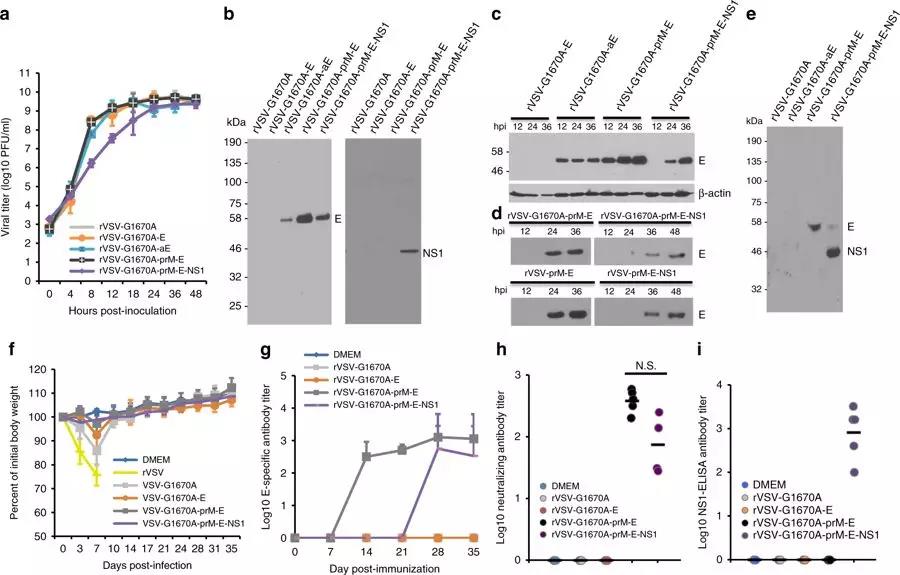
Fig. 2 ZIKV antigen expression and antibody response by MTase-defective rVSV (mtdVSV) vector.
3.进一步的细胞免疫检测结果发现,共表达NS1的重组mtdVSV在BALB/c 小鼠中可诱发ZIKV特异性T细胞免疫反应。prM、E、NS1共表达诱导的Th2和Th17细胞因子反应与prM-E相比水平显著升高(Fig 3)。
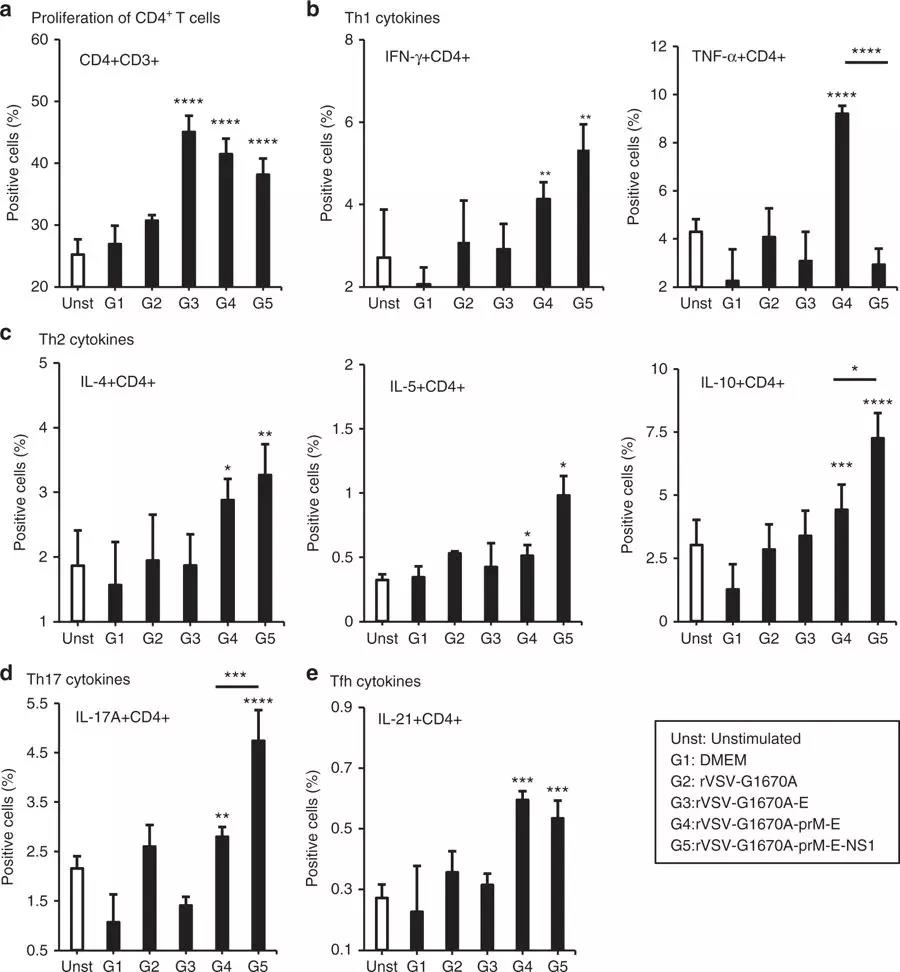
Fig. 3 MTase-defective rVSV (mtdVSV)-based vaccine induces ZIKV-specific T helper cell responses.
4. 为了评估疫苗的免疫保护效果,作者以质粒DNA疫苗pCI-prM-E(2针免疫)为对照,对mtdVSV疫苗在BALB/c小鼠中的免疫效果进行了评估。单针免疫106 PFU的重组病毒疫苗,并以106的寨卡病毒柬埔寨株(FSS13025)进行攻击,结果发现,基于mtdvsvv的疫苗可有效保护BALB/c小鼠免受病毒血症(Fig4)。

Fig. 4 MTase-defective rVSV (mtdVSV)-based vaccine protects BALB/c mice from viremia
5. 为了进一步评估疫苗的免疫保护效果,作者以质粒DNA疫苗pCI-prM-E、pCI-NS1为对照,对突变载体疫苗VSV-G1670A-prM-E-NS1、rVSV-G1670A-prM-E、rVSV-prM-E-NS1在I型干扰素缺失的A129小鼠中进行评估。单针免疫105PFU的重组病毒疫苗,并以106的寨卡病毒柬埔寨株(FSS13025)进行攻击。结果发现,基于mtdvv的疫苗在A129小鼠中可诱导ZIKV特异性体液免疫反应,并提供完全的保护(Fig5,7)。此外,对单独NS1在免疫反应和免疫保护中的作用探讨结果表明,虽然NS1不能诱导中和抗体,但能够对小鼠的ZIKV感染提供部分保护(Fig6,7)。对rVSV-prM-E-NS1 在 A129小鼠中免疫保护效果研究表明,该疫苗不仅具有良好的减毒性,还能完全保护小鼠免受ZIKV的攻击(Fig8)。
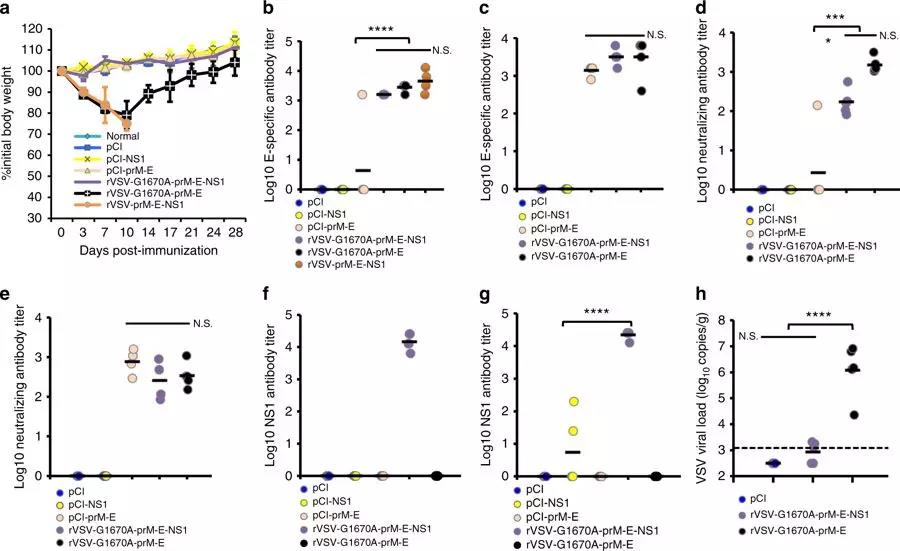
Fig. 5 MTase-defective rVSV (mtdVSV)-based vaccine induces high levels of ZIKV-specific antibody in A129 mice.
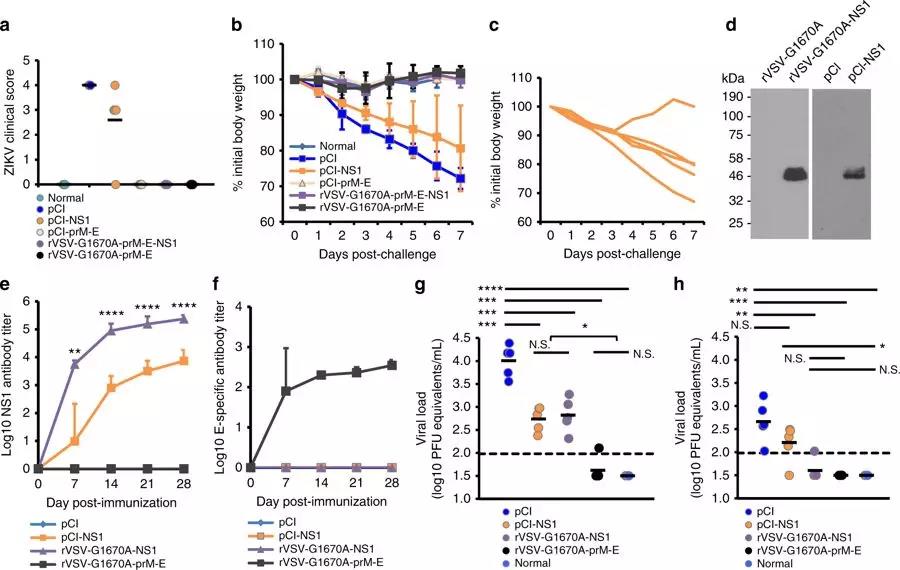
Fig. 6 NS1 alone provides partial protection against ZIKV challenge
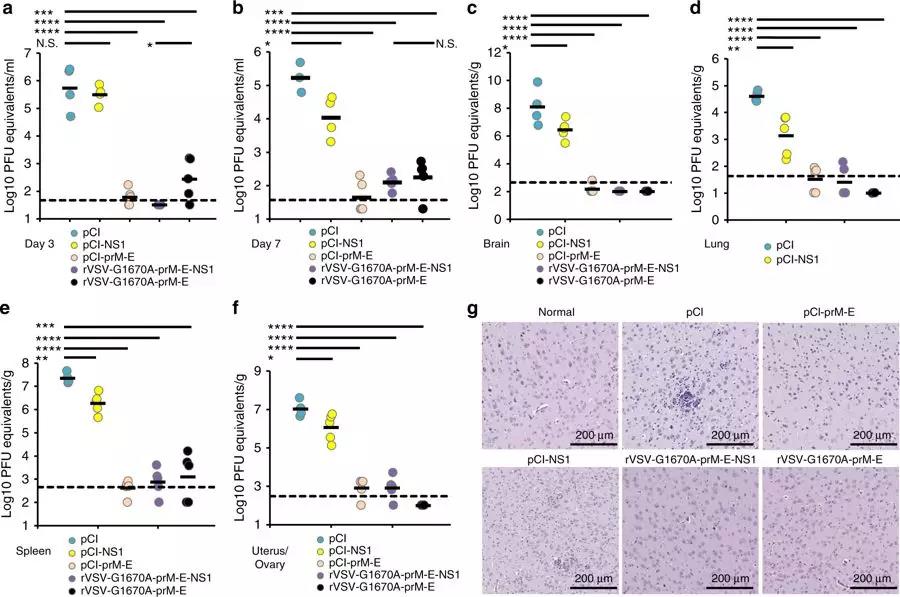
Fig. 7 MTase-defective rVSV (mtdVSV)-based vaccine protects A129 mice from viremia and prevents ZIKV replication in vivo.
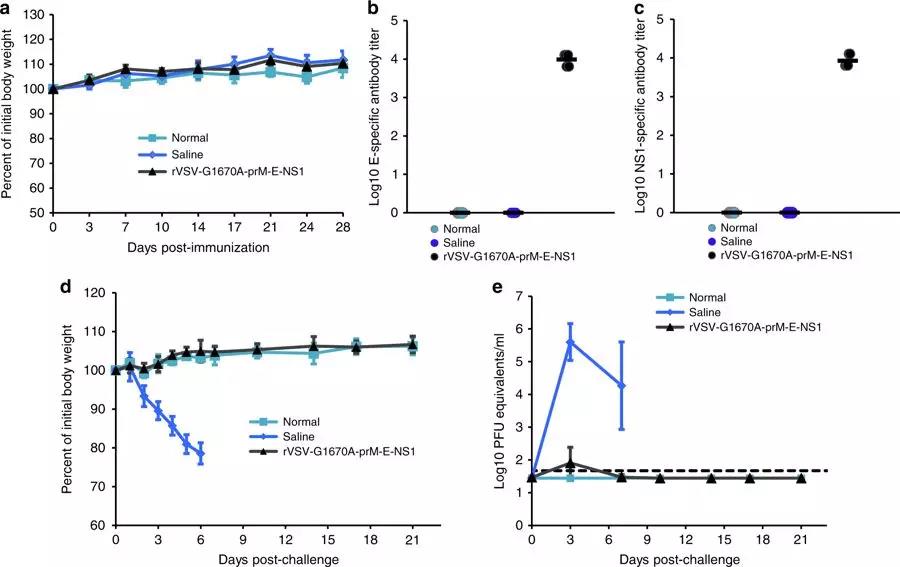
Fig. 8 Validation the safety and immunogenicity of rVSV-prM-E-NS1 in A129 mice.
结语
综上,研究者研发了一种新型的基于mtdvv的病毒载体疫苗,该疫苗共表达寨卡病毒的prM、E、NS1蛋白,该疫苗一针免疫便能在免疫力健全和免疫力缺陷的小鼠模型中均显示出良好的安全性和有效性。
在已有寨卡疫苗靶抗原中增加NS1蛋白,进行多蛋白共表达,这是寨卡疫苗的一种创新方法,本研究同时也强调了对于ZIKV NS1蛋白在免疫应答和免疫保护中的作用。为进一步探讨该疫苗在人体的免疫效果奠定了基础。
ABSTRACT
Current efforts to develop Zika virus (ZIKV) subunit vaccines have been focused on pre-membrane (prM) and envelope (E) proteins, but the role of NS1 in ZIKV-specific immune response and protection is poorly understood. Here, wedevelop an attenuated recombinant vesicular stomatitis virus (rVSV)-based vaccine expressing ZIKV prM-E-NS1 as a polyprotein. This vectored vaccine candidate is attenuated in mice, where a single immunization induces ZIKV-specific antibody and T cell immune responses that provide protectionagainst ZIKV challenge. Co-expression of prM, E, and NS1 induces significantly higher levels of Th2 and Th17 cytokine responses than prM-E. In addition, NS1 alone is capable of conferring partial protection against ZIKV infection inmice even though it does not induce neutralizing antibodies. These results demonstrate that attenuated rVSV co-expressing prM, E, and NS1 is a promising vaccine candidate for protection against ZIKV infection and highlights an important role for NS1 in ZIKV-specific cellular immune responses.
参考文献:
1. LiA, Yu J, Lu M, Ma Y, Attia Z, Shan C, Xue M, Liang X, Craig K, Makadiya N, HeJJ, Jennings R, Shi PY, Peeples ME, Liu SL, Boyaka PN, Li J. AZika virus vaccine expressing premembrane-envelope-NS1 polyprotein. NatCommun. 2018 Aug 3;9(1):3067.
doi:10.1038/s41467-018-05276-4.
内容来源:病毒学界